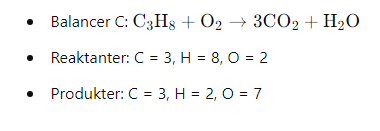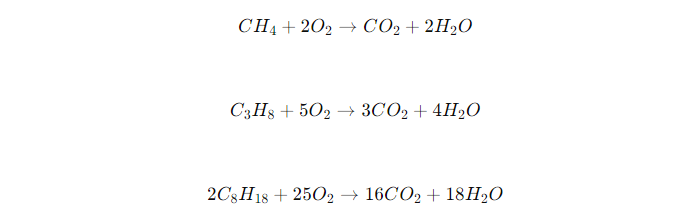Udvidet forklaring
Balancering i kemi refererer til processen med at justere koefficienterne i en kemisk ligning, så antallet af atomer af hver slags er det samme på både reaktant- og produktsiden af ligningen. Dette er nødvendigt for at opfylde loven om bevarelse af masse, som siger, at masse ikke kan skabes eller ødelægges i en kemisk reaktion. Her er en dybdegående forklaring af, hvad balancering indebærer:
Grundprincipper for Balancering
- Bevarelse af Masse:
- Ifølge loven om bevarelse af masse skal den samlede masse af reaktanter være lig med den samlede masse af produkter. Det betyder, at antallet af atomer af hvert grundstof skal være det samme på begge sider af den kemiske ligning.
- Koefficienter:
- Koefficienter er de tal, der placeres foran kemiske formler i en ligning for at angive det antal molekyler eller mol af stoffet, der er involveret i reaktionen. Disse koefficienter justeres under balanceringen.
- Subskripter:
- Subskripter er de små tal, der er en del af de kemiske formler og angiver antallet af atomer af et bestemt grundstof i et molekyle. Disse ændres ikke under balanceringen, da det ville ændre stoffets identitet.
Trin-for-Trin Balanceringsproces
- Skriv den Ubalance Chemiske Ligning:
Start med at skrive den kemiske reaktion med de korrekte kemiske formler for reaktanter og produkter. - Eksempel:
- Tæl Antallet af Atomer:
- Tæl antallet af atomer af hvert grundstof på begge sider af ligningen.
- Eksempel:
- Reaktanter: C = 3, H = 8, O = 2
- Produkter: C = 1, H = 2, O = 3 (fra CO₂ og H₂O)
- Juster Koefficienterne:
- Start med det grundstof, der forekommer færrest gange. Juster koefficienterne for at få lige mange atomer på begge sider.
- Eksempel:

- Kontrollér Ligningen:=
- Tjek igen for at sikre, at antallet af atomer af hvert grundstof er ens på begge sider af ligningen.
Praktiske Tips
- Balancer først grundstoffer, der kun forekommer i én forbindelse på hver side af ligningen.
- Gem grundstoffer, der forekommer i flere forbindelser, eller som frie elementer til sidst.
- Hvis du har et ulige antal af et atom på én side og et lige antal på den anden, kan du midlertidigt bruge brøker som koefficienter og derefter multiplicere hele ligningen for at fjerne brøkerne.
Eksempel på Kompleks Balancering
For en mere kompleks reaktion som forbrænding af ammoniak:
![]()
- Skriv og tæl atomer:
- Reaktanter: N = 1, H = 3, O = 2
- Produkter: N = 1, H = 2, O = 3
- Balancer N og H:
- Reaktanter: N = 4, H = 12, O = 2
- Produkter: N = 4, H = 12, O = 14
- Balancer O:
- Reaktanter: N = 4, H = 12, O = 14
- Produkter: N = 4, H = 12, O = 14
Ved at følge disse trin og principper sikrer balancering, at den kemiske ligning er korrekt i overensstemmelse med loven om bevarelse af masse, hvilket er fundamentalt for forståelsen af kemiske reaktioner.
Optimer dit sprog - Læs vores guide og scor topkarakter
Hvordan kan Balancering bruges i en gymnasieopgave?
Hvordan kan Balancering bruges i en gymnasieopgave?
Balancering af kemiske ligninger kan anvendes i en gymnasieopgave til at illustrere forståelsen af kemiske reaktioner, bevaring af masse, og stoikiometri. Her er nogle måder, hvorpå balancering kan integreres i forskellige typer gymnasieopgaver:
- Kemiske Reaktionsrapporter
Når elever skal skrive rapporter om kemiske eksperimenter, er balancering af de involverede reaktioner afgørende. De kan:- Angive de korrekte kemiske ligninger: Elever kan inkludere både de ubalancerede og balancerede ligninger for at vise deres forståelse af processen.
- Diskutere betydningen af balancering: Forklare, hvorfor det er nødvendigt at balancere ligninger for at overholde loven om bevarelse af masse.
- Illustrere eksperimentelle resultater: Brug balancerede ligninger til at vise de forventede produkter og sammenligne dem med de faktiske eksperimentelle data.
- Stoikiometriske Beregninger
Balancering er grundlaget for stoikiometri, som omfatter beregninger af mængder af reaktanter og produkter i kemiske reaktioner. Elever kan:- Beregn molmængder: Brug balancerede ligninger til at bestemme, hvor mange mol af hver reaktant der er nødvendige for at producere en given mængde produkt.
- Bestemme teoretisk udbytte: Beregn det maksimale mulige udbytte af en reaktion ved hjælp af balancerede ligninger og sammenligne dette med det faktiske udbytte fra eksperimentet.
- Løs begrænsende reaktant-problemer: Identificere den begrænsende reaktant i en reaktion og beregne, hvor meget af de andre reaktanter der vil blive forbrugt, og hvor meget produkt der vil blive dannet.
- Kvantitative Analyser
I opgaver, der involverer kvantitativ analyse af kemiske reaktioner, kan elever bruge balancerede ligninger til:- Titreringer: Beregne koncentrationer af opløsninger ved hjælp af balancerede ligninger for neutraliseringsreaktioner.
- Gasudviklingsreaktioner: Beregn volumenet af gas, der udvikles i en reaktion, ved hjælp af idealgasloven og balancerede ligninger.
- Termokemi: Beregn entalpiforandringer ved kemiske reaktioner ved at bruge balancerede ligninger til at finde mængden af reaktanter og produkter involveret i en reaktion.
- Miljøkemi
I miljørelaterede opgaver kan elever bruge balancering til at analysere:- Forureningskilder: Balancere reaktioner for at forstå processerne bag produktionen af forurenende stoffer, såsom svovldioxid og nitrogenoxider i forbrændingsreaktioner.
- Rensningsprocesser: Balancere reaktioner i vandbehandling og luftkvalitetsforbedring for at vise, hvordan forurenende stoffer kan neutraliseres eller fjernes.
- Klimaændringer: Balancere reaktioner involveret i kulstofkredsløbet for at forstå, hvordan menneskelig aktivitet påvirker koncentrationen af drivhusgasser i atmosfæren.
- Projektarbejde og Præsentationer
Når elever arbejder på projekter eller forbereder præsentationer, kan de inkludere balancerede ligninger til at:- Visualisere kemiske processer: Brug balancerede ligninger i præsentationer for at illustrere, hvordan specifikke kemiske processer fungerer.
- Understøtte argumenter: Inkludere balancerede ligninger som bevis for påstande om kemiske reaktioner i projektrapporter.
- Engagere publikum: Demonstrere balancering i praksis som en del af interaktive præsentationer eller laboratoriedemonstrationer.
Eksempel på en Gymnasieopgave
Forestil dig, at elever arbejder på en opgave om forbrændingsreaktioner af fossile brændstoffer og deres miljøpåvirkning. De kunne:
- Introduktion: Forklare hvad forbrændingsreaktioner er, og hvorfor de er vigtige.
- Balancerede ligninger: Inkludere balancerede ligninger for forbrændingen af forskellige fossile brændstoffer, f.eks. metan (CH4CH_4CH4), propan (C3H8C_3H_8C3H8), og benzin (C8H18C_8H_{18}C8H18).
- Miljøpåvirkning: Diskutere, hvordan produktionen af CO2CO_2CO2 fra disse reaktioner bidrager til drivhuseffekten og global opvarmning.
- Kvantiative beregninger: Beregn hvor meget CO2CO_2CO2 der produceres ved forbrænding af en given mængde af hvert brændstof.
- Løsninger: Undersøge alternative energikilder og balancere reaktioner for brændselsceller eller biodiesel som mere miljøvenlige alternativer.
Ved at integrere balancering i deres opgaver, viser eleverne deres forståelse af fundamentale kemiske principper og deres evne til at anvende disse principper i praktiske og teoretiske sammenhænge.